HemaBook hoofdstuk 9: Hoe verandert het aantal eosinofielen bij COVID-19-patiënten?
Mindray 2021-05-09

Is profylactische antistollingstherapie een gebruikelijke behandeling voor clinici om trombotische voorvallen in COVID-19 aan te pakken?
Is er een verband tussen het aantal eosinofielen en antistollingsmonitoring bij COVID-19-patiënten?
Trombotische voorvallen bij COVID-19-patiënten
Trombose is naar voren gekomen als een belangrijke complicatie bij ziekenhuispatiënten met COVID-19. Een protrombotische toestand geïnduceerd door SARS-Cov-2 kan zich uiten in veneuze trombo-embolie (VTE), arteriële trombose en diffuse intravasale stolling (DIS).[1]
In 28 onderzoeken met 2928 patiënten traden trombotische complicaties op bij 34% van de IC-patiënten. Diepe veneuze trombose (DVT) werd gemeld bij 16,1% en longembolie bij 12,6% van de patiënten. Al deze complicaties waren geassocieerd met een hoge mortaliteit.[2]
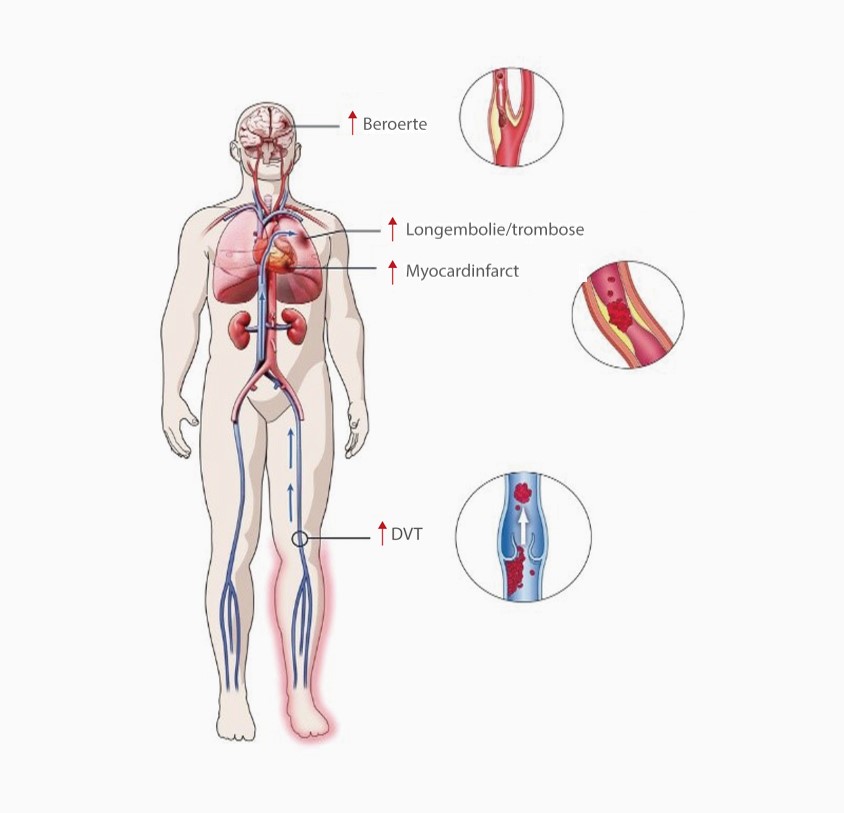
Antitrombotische behandeling met laagmoleculairgewicht heparine bij COVID-19-patiënten
Laagmoleculairgewicht heparine (LMWH) en ongefractioneerde heparine (UFH) worden aanbevolen door de International Society for Thrombosis on Hemostasis (ISTH), American Society of Hematology (ASH) voor de behandeling van trombotische voorvallen die verband houden met een SARS-CoV-2-infectie. Met name LMWH heeft een sterker antitrombotisch effect dan UFH.
LMWH-dosisbewaking
LMGH werkt voornamelijk in op factor Xa. Om deze reden wordt de LMWH-activiteit gevolgd met behulp van serum-anti-factor Xa-activiteitsniveaus (AFXa) in plaats van geactiveerde partiële tromboplastinetijd (aPTT) (Figuur 2).[3]
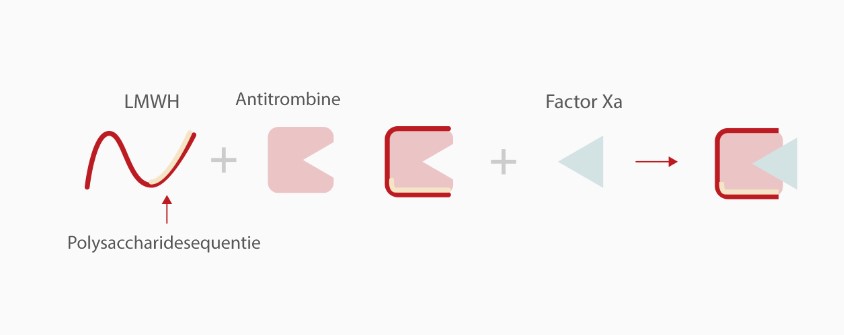
Enoxaparine is een van de belangrijkste LMWH. Het AFXa-niveau bereikte zijn piek 3-5 uur na toediening. De AFXa-waarden lager dan 0,2 IE/ml kunnen het risico op VTE bij COVID-19-patiënten verhogen vanwege de hypercoagulabiliteit.[4]
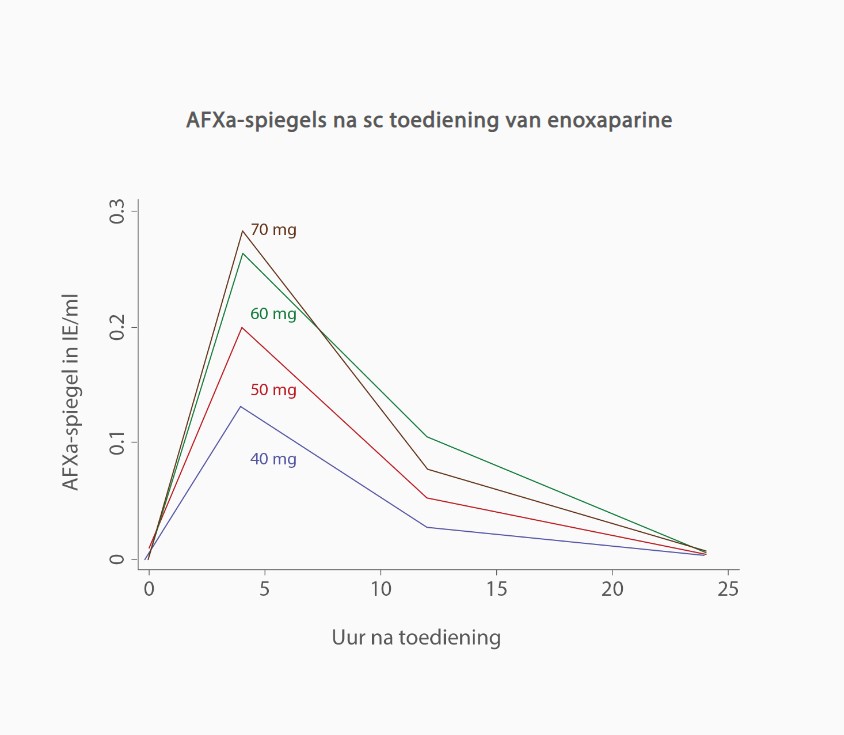
Eosinofielenaantallen bij antitrombotische behandeling van COVID-19 patiënten
Dr. Selma Ari heeft ontdekt dat het verhoogde aantal eosinofielen samenhangt met de mate van subprofylactische antistolling bij COVID-19-patiënten.[5]
In de laboratoriumresultaten zijn alleen het aantal eosinofielen en AFXa significant verschillend tussen de subprofylactische antistollingsgroep en de profylactische antistollingsgroep wanneer de patiënten in het ziekenhuis zijn opgenomen (tabel 1).[5]
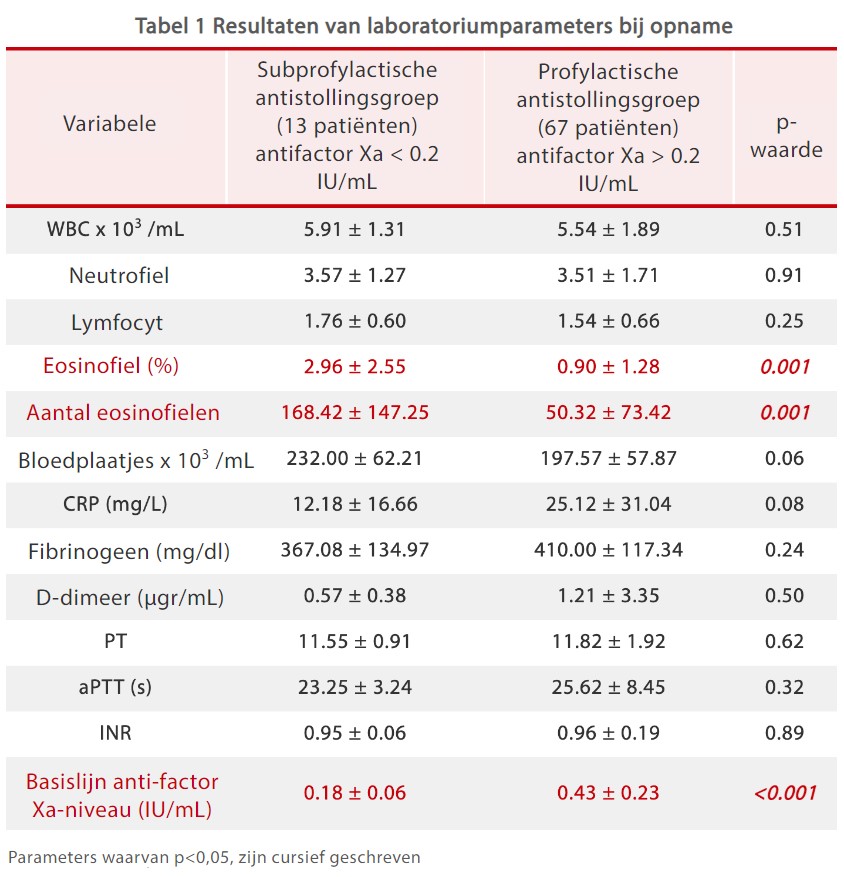
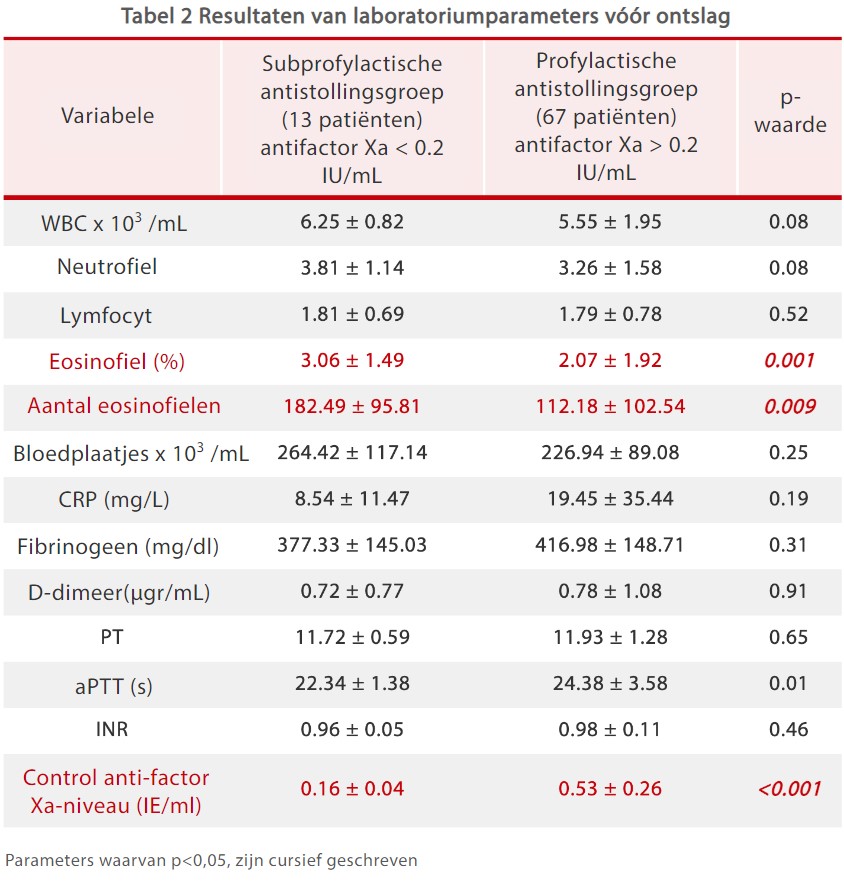
Laboratoriumanalyses verzameld vóór het ontslag van de patiënten toonden aan dat het aantal eosinofielen in de subprofylactische antistollingsgroep hoger waren dan in de profylactische antistollingsgroep , terwijl AFXa lager was in subprofylactische antistollingsgroep (tabel 2).[5]
Eosinofielen en trombose
Eosinofiel veroorzaakt bloedplaatjesaggregatie en trombusvorming door de productie van major basic protein (MBP) en eosinofielperoxidase (EPX).[6]
Enzymen die vrijkomen uit eosinofielen (peroxidases, kationische eiwitten, en neurotoxines) kunnen de antistollingsactiviteit van heparine verminderen.[7]
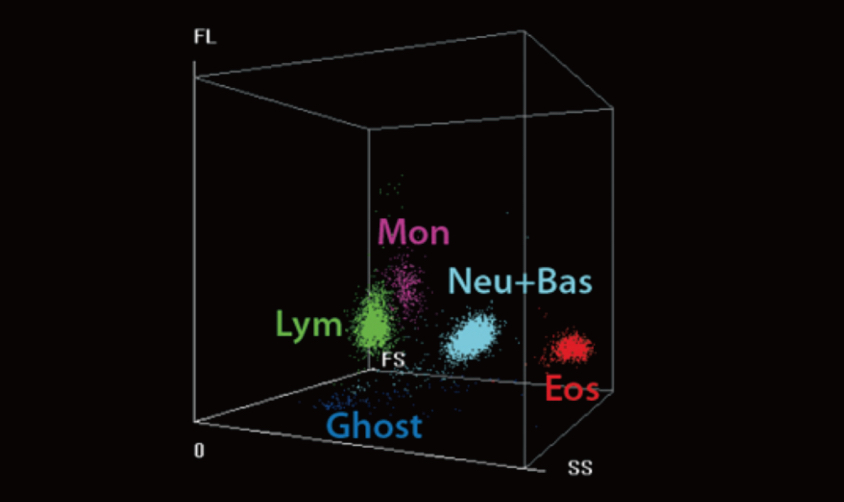
In deze studie, in de subprofylactische antistollingsgroep, hadden hoge eosinofieleniveaus een lagere antistollingsactiviteit bij COVID-19-patiënten. Het aantal eosinofielen werd onderzocht met de Mindray BC-6800 Auto-hematologieanalysator. De SF Cube-analysetechnologie kan een driedimensionaal scattergram produceren dat artsen kan helpen bloedcelpopulaties beter te identificeren en te differentiëren, met name om abnormale celpopulaties aan het licht te brengen die met andere technieken niet worden gedetecteerd. Tegenwoordig kan een groot aantal parameters op BC-6800 worden gebruikt bij klinische diagnose en wetenschappelijk onderzoek. Daarom zijn clinici welkom om meer onderzoek te doen naar COVID-19 op Mindray BC-6200/BC-6800/BC-6800Plus/CAL 6000/CAL 8000.
Referenties:
[1] Godoy, L. C., Goligher, E. C., Lawler, P. R., Slutsky, A. S. & Zarychanski, R. Anticipating and managing coagulopathy and thrombotic manifestations of severe COVID-19. CMAJ 192, E1156-E1161, doi:10.1503/cmaj.201240 (2020).
[2] Jenner, W. J. et al. Thrombotic complications in 2928 patients with COVID-19 treated in intensive care: a systematic review. J Thromb Thrombolysis, doi:10.1007/s11239-021-02394-7 (2021).
[3] Lai, S. & Coppola, B. Use of enoxaparin in end-stage renal disease. Kidney Int 84, 433-436, doi:10.1038/ki.2013.163 (2013).
[4] Robinson, S. et al. Enoxaparin, effective dosage for intensive care patients: double-blinded, randomised clinical trial. Crit Care 14, R41, doi:10.1186/cc8924 (2010).
[5] Ari, S. et al. Elevated eosinophil count is related with lower anti-factor Xa activity in COVID-19 patients. J Hematop, 1-10, doi:10.1007/s12308-020-00419-3 (2020).
[6] Varricchi, G. et al. Reslizumab and Eosinophilic Asthma: One Step Closer to Precision Medicine? Front Immunol 8, 242, doi:10.3389/fimmu.2017.00242 (2017).
[7] Ames, P. R., Aloj, G. & Gentile, F. Eosinophilia and thrombosis in parasitic diseases: an overview. Clin Appl Thromb Hemost 17, 33-38, doi:10.1177/1076029609348314 (2011).







