Klinische belang van Lipide Analyse in CKD Management
Mindray 2021-06-09


Het wordt algemeen aanvaard dat laboratoriumonderzoek naar het lipidenmetabolisme klinisch significant is voor het inschatten van het risico op atherosclerotische cardiovasculaire ziekte (ASCVD) en therapeutische besluitvorming. Zoals aanbevolen door de 2019 ESC/EAS Richtlijnen voor de behandeling van dyslipidemieën, zijn plasmalipideanalyse (bijv. TG, TC, HDL-C, LDL-C, apo B, Lp(a), enz.) en juiste behandeling zinvolle manieren om het risico op ASCVD-gebeurtenissen te verminderen.[1]

Chronische nierziekte (CKD) is een van 's werelds grootste gezondheidsproblemen. De geschatte prevalentie van CKD is 13,4% (11,7%-15,1%), en er wordt geschat dat er wereldwijd tussen de 4,9 miljoen en 7,1 miljoen patiënten zijn met nierziekte in het eindstadium die niervervangende therapie nodig hebben.[2]
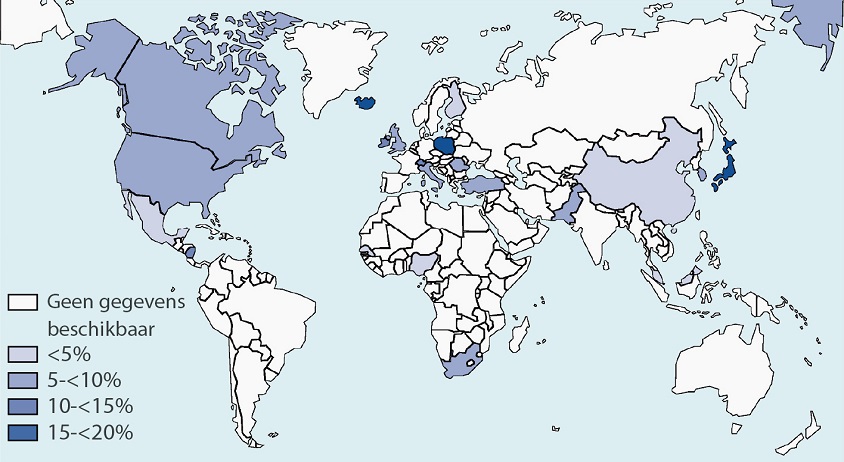
De meeste patiënten met CKD lopen risico op versnelde hart- en vaatziekten en overlijden, en veel van de cardiovasculaire comorbiditeiten kunnen verband houden met dyslipidemie, hoewel er significante verschillen zijn in termen van populatie, de etiologie van nierschade, de stadia van ziekteprogressie en de therapeutische interventies. Het niveau, de samenstelling en de kwaliteit van plasmalipiden kunnen worden beïnvloed door de veranderde nierfunctie. Het kenmerkende lipidenpatroon in patiënten met CKD stadium 3 of hoger bestaat uit hypertriglyceridemie, lage niveaus van HDL-cholesterol, lage niveaus van Apo A1 en variabele niveaus van LDL-cholesterol en totaal cholesterol. Lp(a)-niveaus kunnen ook toenemen in verband met CKD.[1,4]
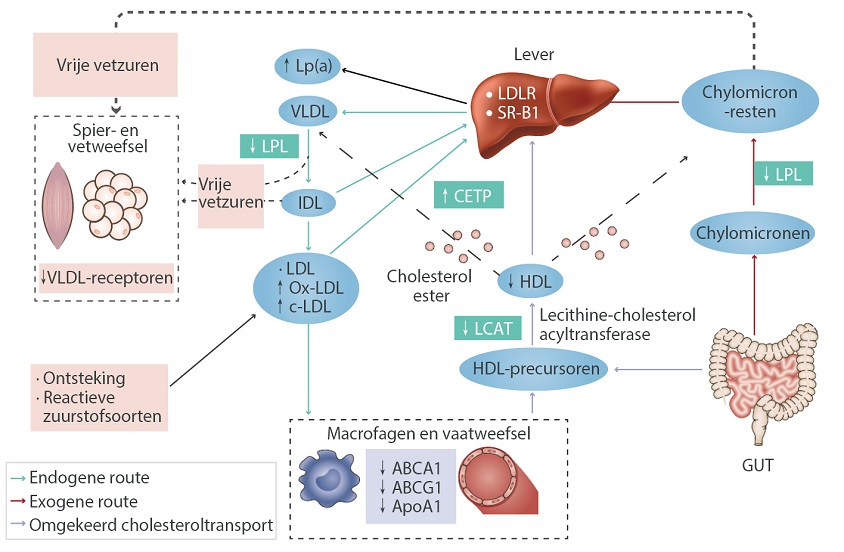
Hypertriglyceridemie bij CKD is het gevolg van het vertraagde katabolisme van triglyceride-rijke lipoproteïnen. De synthese van Apo A1 is verminderd in patiënten met CKD, en de activering van LCAT door Apo A1 is ook verminderd. De rijping van HDL-precursoren wordt bijgevolg beïnvloed. Verhoogd Lp(a) wordt veroorzaakt door post-translatie modificatie van lipoproteïnen die verband houden met CKD.
Dientengevolge wordt, vanwege de relatie tussen CKD en dyslipidemie, lipide-evaluatie voorgesteld om te helpen bij het beheersen van de aandoening voor veel patiënten.
De Nierziekte: De organisatie Improving Global Outcomes (KDIGO) publiceerde in 2013 haar nieuwste richtlijnen. Zoals aanbevolen in de klinische praktijkrichtlijnen, moeten alle volwassenen met nieuw geïdentificeerde CKD (inclusief degenen die worden behandeld met chronische dialyse of niertransplantatie) worden beoordeeld met een lipidenprofiel (TG, TC, LDL-C en HDL-C). Er worden nuchtere lipidenprofieltests aanbevolen, vooral voor patiënten met bekende significante lipidenafwijkingen. Bovendien kan lipidenanalyse voor sommige CKD-patiënten jonger dan 50 jaar helpen bij het starten van statinetherapie en het identificeren van onderliggende secundaire oorzaken van ernstige hypercholesterolemie en/of hypertriglyceridemie.[5]
Bij patiënten die een niertransplantatie hebben ondergaan kunnen dyslipidemieën zeer vaak voorkomen, waardoor ze een hoog risico lopen op ASCVD en arteriële vasculopathie van de transplantatie. Het wordt aanbevolen dat deze patiënten worden beoordeeld op hun risico op het ontwikkelen van ASCVD, en een volledige lipidenanalyse is hierbij nuttig. Als het lipidenprofiel terugkeert naar een meer normaal patroon en deze verandering aanhoudt, kan het risico op ASCVD aanzienlijk worden verminderd.[6,7]
Omgekeerd wordt vanwege het gebrek aan direct bewijs monitoring van het lipidenniveau niet gesuggereerd door de KDIGO-werkgroep (2013) bij CKD-patiënten met verminderde GFR, in tegenstelling tot de LDL-C-surveillance die onderdeel is van de behandeling van de meeste patiënten. Aangezien een lage GFR een onafhankelijke risicofactor is voor ASCVD, zou een strikte lipidenverlagende therapie de medische behandeling niet veranderen en het risico op ernstige cardiovasculaire gebeurtenissen niet verminderen.[5]
Sommige onderzoeken hebben echter aangetoond dat het verlagen van LDL-C gunstig is, omdat het het cardiovasculaire risico vermindert van CKD-patiënten die geen dialyse nodig hebben (inclusief ontvangers van een niertransplantatie), terwijl andere richtlijnen suggereren dat de lipiden worden gecontroleerd om ervoor te zorgen dat het streefcijfer voor cholesterolverlaging wordt gehaald.[4] Daarom heeft lipidenanalyse een groot potentieel voor de behandeling van CKD-patiënten: bij het beoordelen van therapietrouw aan statinebehandeling, veranderingen in de modaliteit van nierfunctievervangende therapie of bezorgdheid over de aanwezigheid van een nieuwe secundaire oorzaak van dyslipidemie, en zelfs het beoordelen van het 10-jarige cardiovasculaire risico bij patiënten van < 50 jaar die momenteel geen statine krijgen.[5]
Samenvattend: lipidenanalyse speelt een cruciale rol bij het verminderen van ASCVD-risico's, hoewel het testen van lipiden behoorlijk gecompliceerd is bij patiënten met CKD, een veel voorkomende medische aandoening wereldwijd. Alle patiënten met nieuw geïdentificeerde CKD moeten een lipidenanalyse ondergaan en veel van deze patiënten zouden baat kunnen hebben bij medische interventie op basis van lipidenmonitoring.
Referenties:
[1] François Mach, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. European Heart Journal, 2020(1)41, 111–188, https://doi.org/10.1093/eurheartj/ehz455
[2] Lv JC, Zhang LX. Prevalence and Disease Burden of Chronic Kidney Disease. Adv Exp Med Biol. 2019; 1165:3-15. doi: 10.1007/978-981-13-8871-2_1
[3] Webster, A., Nagler, E., Morton, R. et al. Chronic kidney disease.The Lancet. 2017; 389: 1238-1252. https://doi.org/10.1016/S0140-6736(16)32064-5
[4] Ferro, C.J., Mark, P.B., Kanbay, M. et al. Lipid management in patients with chronic kidney disease.Nat Rev Nephrol. 14, 727–749 (2018). https://doi.org/10.1038/s41581-018-0072-9
[5] Wanner C, Tonelli M, et al. KDIGO Clinical Practice Guideline for Lipid Management in CKD: summary of recommendation statements and clinical approach to the patient. Kidney Int. 2014 Jun;85(6):1303-9. doi: 10.1038/ki.2014.31
[6] JJennifer L Larsen, et al. Lipid Status After Pancreas-Kidney Transplantation. Diabetes Care Jan. 1992, 15 (1) 35-42; DOI: 10.2337/diacare.15.1.35
[7] Claudio Ponticelli, et al. Treatment of dyslipidemia in kidney transplantation. Expert Opinion on Drug Safety. (2020) 19 :3, 257-267, DOI: 10.1080/14740338.2020.1732921





