Importancia clínica del análisis de lípidos en el tratamiento de la Enfermedad renal Crónica (ERC)
Mindray 2021-06-09


Está ampliamente aceptado que la investigación del laboratorio en metabolismo de los lípidos es clínicamente significativa para estimar el riesgo de enfermedad cardiovascular aterosclerótica (ECVA) y guiar la toma de decisiones terapéuticas. Según lo recomendado por las Guías de la ESC/EAS de 2019 para el tratamiento de las dislipidemias, el análisis de lípidos plasmáticos (p. ej., TG, CT, C-HDL, C-LDL, apo B, Lp(a), etc.) y el tratamiento adecuado son formas significativas para reducir el riesgo de eventos de ECVA.[1]

La enfermedad renal crónica (ERC) es uno de los principales problemas de salud del mundo. La prevalencia estimada de ERC es del 13,4 % (11,7 a 15,1 %) y se estima que en el mundo hay entre 4,9 millones y 7,1 millones de pacientes con enfermedad renal en etapa terminal que necesitan terapia de reemplazo renal.[2]
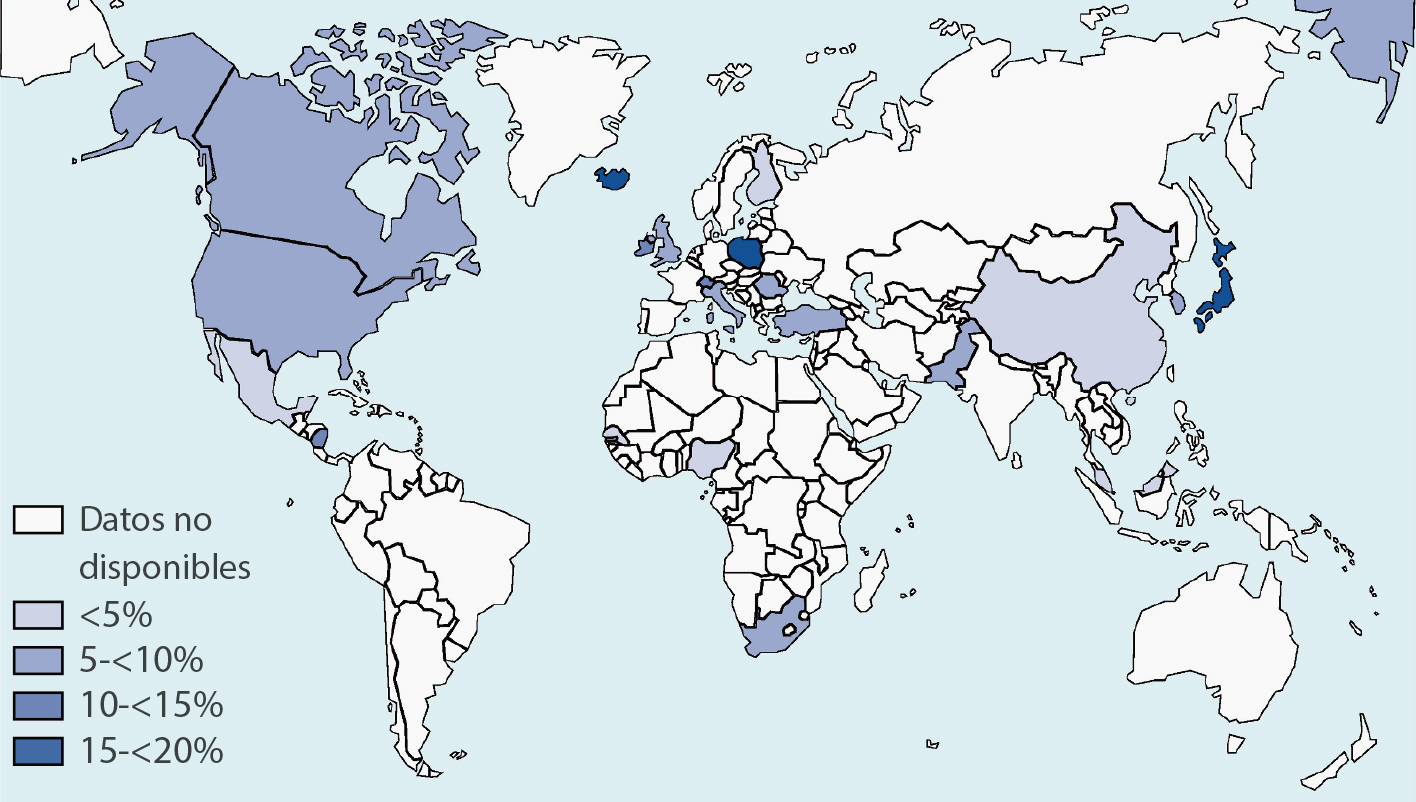
La mayoría de los pacientes con enfermedad renal crónica están en riesgo de sufrir enfermedad cardiovascular acelerada y muerte, y muchas de las comorbilidades cardiovasculares podrían estar relacionadas con dislipidemias, aunque existen diferencias significativas en términos de población, etiologías del daño renal, etapas de progresión de la enfermedad y las intervenciones terapéuticas. La función renal alterada podría afectar el nivel, la composición y la calidad de los lípidos plasmáticos. El patrón lipídico característico en pacientes con ERC en etapa 3 o superior consiste en hipertrigliceridemia, niveles bajos de colesterol HDL, niveles bajos de Apo A1 y niveles variables de colesterol LDL y colesterol total. Los niveles de Lp(a) también podrían aumentar en asociación con la ERC.[1,4]
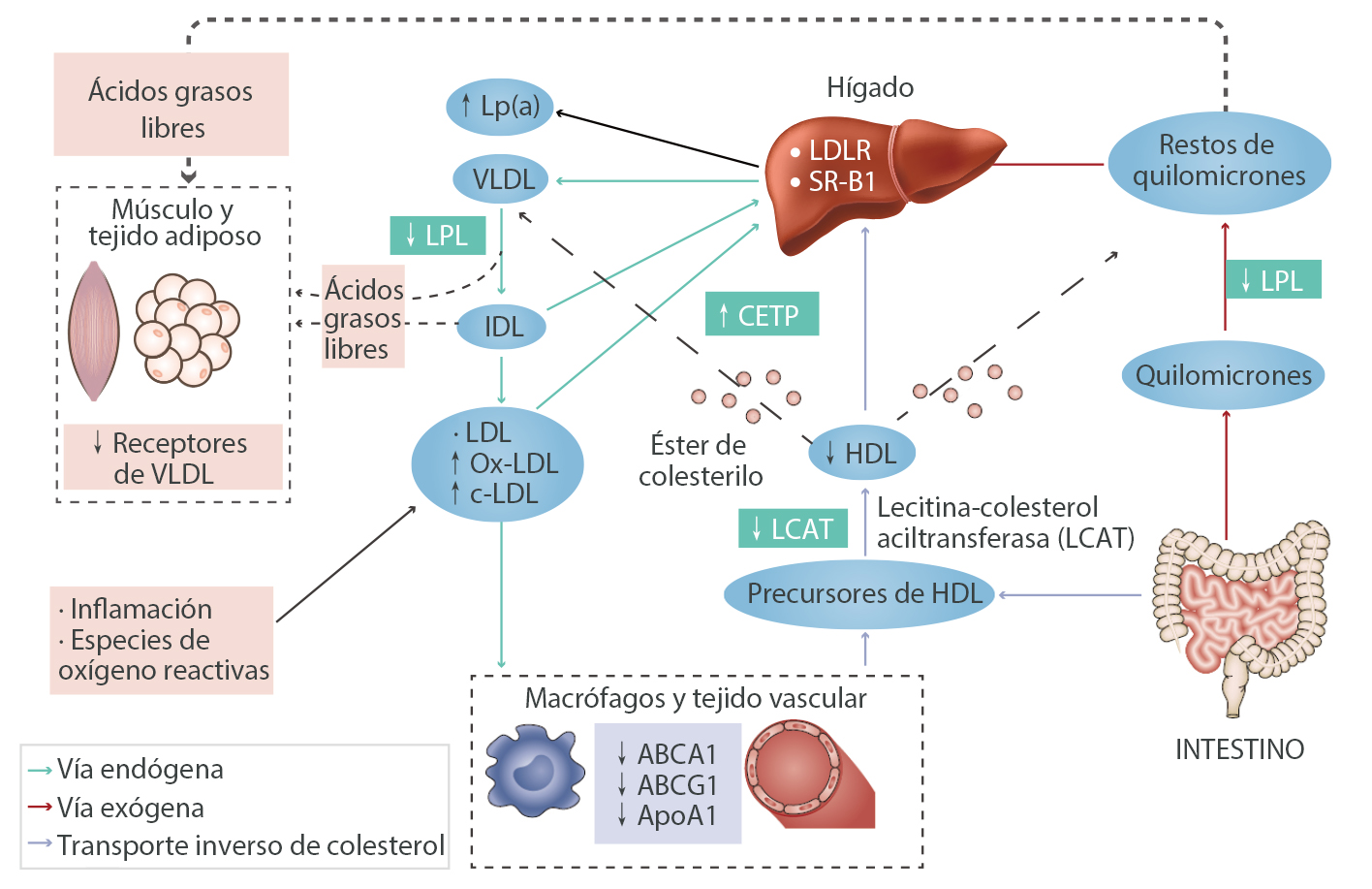
La hipertrigliceridemia en la enfermedad renal crónica se debe al catabolismo retardado de las lipoproteínas ricas en triglicéridos. La síntesis de Apo A1 se reduce en pacientes con ERC y la activación de LCAT por Apo A1 también se ve disminuida. En consecuencia, la maduración de los precursores de HDL es afectada. El aumento de Lp(a) está causado por la modificación posterior a la traducción de las lipoproteínas relacionadas con la ERC.
En consecuencia, debido a la relación entre la ERC y la dislipidemia, la evaluación de lípidos es sugerida para ayudar a manejar la afección en muchos pacientes.
La enfermedad renal: La organización Improving Global Outcomes (KDIGO) publicó sus últimas directrices en 2013. Como se recomienda en las guías de práctica clínica, todos los adultos a quienes se les haya identificado con ERC recientemente (incluyendo aquellos tratados con diálisis crónica o trasplante renal) deben ser evaluados con un perfil lipídico (TG, CT, C-LDL y C-HDL). Se sugieren las pruebas de perfil lipídico en ayunas, especialmente para pacientes con anomalías lipídicas significativas conocidas. Adicionalmente, para algunos pacientes menores de 50 años con ERC, el análisis de lípidos podría ayudar a iniciar el tratamiento con estatinas e identificar cualquier causa secundaria subyacente de hipercolesterolemia grave o hipertrigliceridemia.[5]
Para los pacientes a los que se les ha realizado un trasplante de riñón, las dislipidemias podrían ser muy comunes, lo que los pondría en alto riesgo de enfermedad cardiovascular ateroesclerótica y vasculopatía arterial por trasplante. Se recomienda que estos pacientes sean evaluados por su riesgo de desarrollar ECVA, y es útil un análisis de lípidos completo. Si el perfil de lípidos regresa a un patrón más normal y dichos cambios se mantienen, el riesgo de ECVA podría reducirse de manera significativa.[6,7]
Por el contrario, a diferencia de la vigilancia de C-LDL involucrada en el tratamiento de la mayoría de los pacientes, el grupo de trabajo KDIGO (2013) no sugiere el monitoreo del nivel de lípidos en pacientes con ERC con tasa de filtrado glomerular (TFG) disminuida debido a la falta de evidencia directa. Dado que la TFG baja es un factor de riesgo independiente de ECVA, la terapia de reducción de lípidos estricta no cambiaría el tratamiento médico ni reduciría el riesgo de episodios cardiovasculares importantes.[5]
Sin embargo, algunos ensayos han mostrado que reducir el C-LDL es beneficioso, ya que reduce el riesgo cardiovascular de los pacientes con ERC que no requieren diálisis (incluyendo los receptores de trasplante de riñón), mientras que otras directrices sugieren el control de lípidos para garantizar que se alcance el objetivo de reducción del colesterol.[4]Por lo tanto, el análisis de lípidos tiene un gran potencial en el manejo de los pacientes con ERC: en la evaluación de la adherencia al tratamiento con estatinas, cambios en la modalidad de terapia de reemplazo renal o preocupaciones sobre la presencia de una nueva causa secundaria de dislipidemia, e incluso en la evaluación del riesgo cardiovascular a 10 años en pacientes menores de 50 años que no reciben actualmente una estatina.[5]
En conclusión, el análisis de lípidos juega un papel crucial en la reducción de los riesgos de la enfermedad cardiovascular ateroesclerótica, aunque la prueba de lípidos es bastante complicada en pacientes con enfermedad renal crónica, un problema de salud común en todo el mundo. Todos los pacientes a quienes se les haya identificado con ERC recientemente deben someterse a un análisis de lípidos, y muchos de dichos pacientes podrían beneficiarse de una intervención médica basada en el monitoreo de lípidos.
Referencias:
[1] François Mach, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. European Heart Journal, 2020(1)41, 111–188, https://doi.org/10.1093/eurheartj/ehz455
[2] Lv JC, Zhang LX. Prevalence and Disease Burden of Chronic Kidney Disease. Adv Exp Med Biol. 2019; 1165:3-15. doi: 10.1007/978-981-13-8871-2_1
[3] Webster, A., Nagler, E., Morton, R. et al. Chronic kidney disease.The Lancet. 2017; 389: 1238-1252. https://doi.org/10.1016/S0140-6736(16)32064-5
[4] Ferro, C.J., Mark, P.B., Kanbay, M. et al. Lipid management in patients with chronic kidney disease.Nat Rev Nephrol. 14, 727–749 (2018). https://doi.org/10.1038/s41581-018-0072-9
[5] Wanner C, Tonelli M, et al. KDIGO Clinical Practice Guideline for Lipid Management in CKD: summary of recommendation statements and clinical approach to the patient. Kidney Int. 2014 Jun;85(6):1303-9. doi: 10.1038/ki.2014.31
[6] JJennifer L Larsen, et al. Lipid Status After Pancreas-Kidney Transplantation. Diabetes Care Jan. 1992, 15 (1) 35-42; DOI: 10.2337/diacare.15.1.35
[7] Claudio Ponticelli, et al. Treatment of dyslipidemia in kidney transplantation. Expert Opinion on Drug Safety. (2020) 19 :3, 257-267, DOI: 10.1080/14740338.2020.1732921








