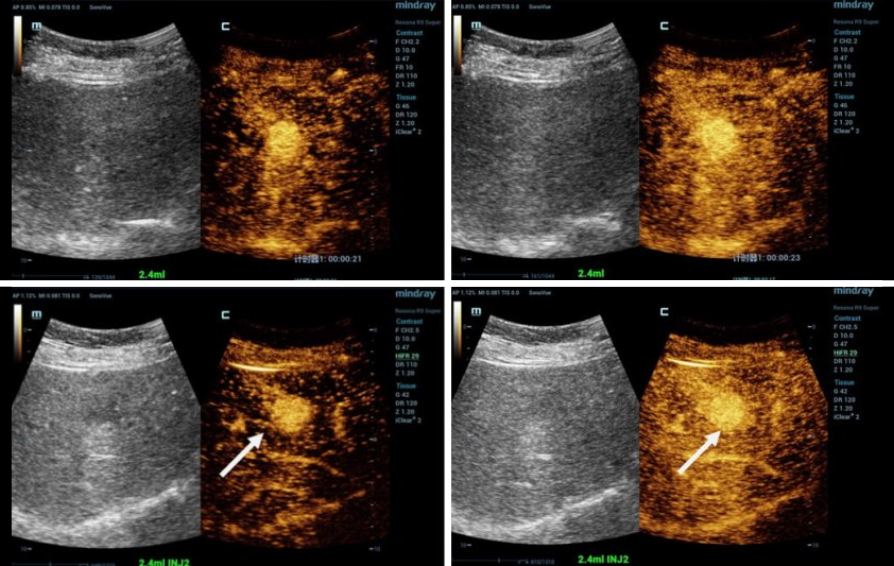
Une étude multicentrique est en cours dans six hôpitaux universitaires dans le but d’évaluer si l'échographie de contraste à haute cadence images (HiFR CEUS) peut distinguer les cancers hépatocellulaires de dimensions réduites d’autres petites lésions hépatiques plus précisément que les méthodes d'échographie conventionnelles.
L'échographie de contraste (CEUS) est un domaine très dynamique et, au cours des dernières années, les innovations technologiques ont encore permis d'améliorer la qualité des images. L'une de ces innovations est l'échographie de contraste améliorée à haute cadence images (HiFR CEUS), en mesure de générer jusqu'à dix fois plus d'images que l'échographie conventionnelle dans le même intervalle de temps. Les chercheurs de sept centres en Allemagne, en Suisse et en Chine évaluent l'efficacité de l’HiFR CEUS dans le diagnostic des petites lésions du foie. Le Dr Yi Dong, du département d'échographie de l'hôpital Xinhua de la faculté de médecine de l'université Jiaotong de Shanghai, et le Dr Christoph F. Dietrich, du département de médecine interne générale de l'hôpital Hirslanden de Berne, en Suisse, expliquent le contexte et les objectifs de l’étude.

Quel est exactement l’objectif de cette étude ?
Yi Dong : « L'objectif principal est un diagnostic plus précis des lésions hépatiques focales d'un diamètre inférieur à 3 cm chez les patients atteints ou non de cirrhose du foie. Les études précédentes ont montré que l’HiFR CEUS permet de visualiser les schémas et la morphologie des vaisseaux dans ces lésions. Nous prévoyons que l’HiFR CEUS offre une meilleure résolution temporelle et spatiale, ou en d'autres termes, des images de meilleure qualité pour les petites lésions hépatiques de dimensions très réduites. Cela permettrait d'accroître la confiance dans la caractérisation et le diagnostic de ces lésions. Des recherches antérieures sur le carcinome hépatocellulaire (CHC) ont montré que le fait que ces petites lésions soient situées dans le fond du foie cirrhotique ou sain fait une grande différence. »
Christoph Dietrich : « Les patients souffrant d'une cirrhose du foie ont un risque élevé et accru de développer un CHC. Les tumeurs de plus de 30 mm chez les patients atteints de cirrhose du foie sont très probablement des CHC. Si le diamètre de la lésion n'est que de 12 mm, la probabilité d'un CHC est réduite à cinquante-cinquante. Par conséquent, la caractérisation des petites tumeurs est plus importante que celle des plus grandes, car celles-ci sont de toute façon très probablement des CHC, ou d'autres diagnostics différentiels aux résultats non ambigus. Si, dans la plupart des cas, le CHC peut faire l'objet d'une ablation chirurgicale, la chirurgie n'est généralement pas indiquée pour les autres tumeurs du foie. Notre objectif est de faire en sorte qu'aucun patient atteint d’une lésion non-CHC, bénigne ou non, ne subisse une intervention chirurgicale inutile. »
Quelle méthode est actuellement utilisée pour caractériser les tumeurs en routine clinique ?
Christoph Dietrich : « Pour déterminer si une intervention chirurgicale est indiquée pour la tumeur, un PET-CT scan du cou au bassin, à savoir la « stadification », est réalisé. En oncologie, l'échographie n'offre pas les mêmes performances que le scanner car, entre autres, elle ne peut pas pénétrer dans le poumon. Le scanner peut être légèrement inférieur à l'échographie pour certains examens des organes abdominaux, mais c'est une méthode de choix fondée sur des faits probants et, dans ce contexte, une procédure tout-en-un. Dans notre étude, nous utilisons l’HiFR CEUS en complément pour voir si une telle échographie apporte des informations supplémentaires pertinentes. Si les preuves scientifiques démontrent que l’HiFR CEUS permet de classifier les petites lésions mieux que le scanner/IRM actuel, le traitement des patients sera amélioré et une chirurgie superflue pourra être évitée. »
Yi Dong : « Nous nous attendons à ce que l’HiFR CEUS surpasse la CEUS conventionnelle dans le diagnostic des lésions focales du foie en ce qui concerne la précision, la sensibilité et la spécificité du diagnostic. Dans cette étude, nous comparons directement les deux méthodes d'imagerie. Cependant, notre objectif n'est pas seulement de montrer que l’HiFR CEUS est supérieure à la CEUS conventionnelle ; nous voulons également identifier les points forts de chacune de ces deux méthodes. »
Christoph Dietrich : « Qu'il s'agisse d'une fréquence d'images élevée ou faible, la CEUS présente un avantage crucial : elle est strictement intravasculaire. Alors que les agents de contraste du scanner agissent à l'extérieur des vaisseaux sanguins, les agents de contraste de l'échographie ne montrent que la vascularisation. »
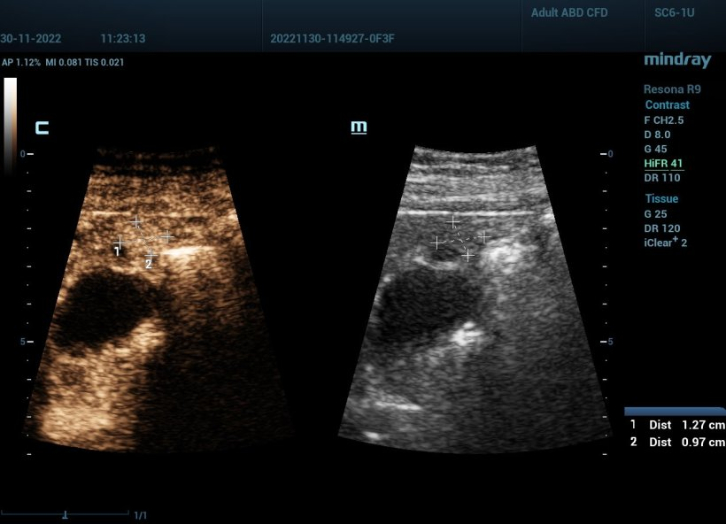
Comment fonctionne cette technologie d’imagerie ?
Yi Dong : « Dans les systèmes d'échographie conventionnels, la fréquence d'images pour l'imagerie de contraste non cardiaque est d'environ dix images par seconde. Le système CEUS HiFR que nous utilisons, Mindray Resona 9, est beaucoup plus rapide : il peut générer jusqu'à 100 images par seconde. Une fréquence d'images aussi élevée offre une meilleure visualisation de la morphologie vasculaire et permet de voir les détails de la perfusion microvasculaire et de mieux suivre le mouvement. En résumé, elle améliore l'efficacité diagnostique CEUS. Dans notre étude, nous nous concentrerons sur l'architecture vasculaire pendant la phase de CEUS artériel, la phase de lavage précoce, le temps d'augmentation du contraste, l'élimination et les modèles pertinents. »
Pourriez-vous nous expliquer cela plus en détail ?
Christoph Dietrich : « Environ 70 % du flux sanguin total du foie passe par la veine porte, qui transporte vers le foie les nutriments et les produits métaboliques provenant du tractus gastro-intestinal, ainsi que les toxines à des fins de détoxification. Le sang artériel fournit également 30 % de l'oxygène. L'échographie de contraste hépatique utilise donc la phase artérielle ainsi que la phase de la veine porte pour générer des images. Dans un foie cirrhotique, la veine porte est endommagée et le sang ne peut plus être détoxifié. Ainsi, en matière d'imagerie, la phase veineuse portale offre moins d'informations. Par conséquent, notre étude se concentrera sur la phase artérielle. Grâce à la fréquence d'images élevée, un grand nombre de données pertinentes sont acquises, bien que la phase de la veine porte ne soit pas prise en compte. C'est comme un filet de pêche : plus le filet est serré, plus on peut attraper de poissons. En matière d’imagerie : plus la densité de lignes est élevée, plus la résolution est élevée. Un plus grand nombre de tumeurs sont détectées et peuvent être traitées conformément aux directives médicales actuelles. »
Pourriez-vous expliquer cela plus en détail ? D'autres technologies innovantes sont-elles utilisées dans l’étude ?
Yi Dong : « Nous utilisons un logiciel particulier appelé VueBox pour effectuer une analyse quantitative des données. Cela nous permet de capturer la courbe d'intensité temporelle et de fournir des paramètres quantitatifs pour les diagnostics futurs. Nous espérons que ces analyses quantitatives nous permettront de détecter plus tôt les petites lésions. »
Christoph Dietrich : « La quantification de la cinétique de rehaussement est un outil prometteur pour rendre l'imagerie plus objective. Après tout, les chiffres fournissent plus d'informations que les simples degrés de luminosité qui sont visibles lors du renforcement et du délavage de l'agent de contraste. »
À l'avenir, l’HiFR CEUS pourrait-elle être utilisée à d’autres fins ?
Yi Dong : « L’HiFR CEUS pourrait faciliter le diagnostic des petites lésions mammaires ou thyroïdiennes et des perfusions microvasculaires des vaisseaux alimentant la carotide. »
Christoph Dietrich : « Ce que nous avons dit précédemment à propos du foie vaut également pour les autres organes : plus la lésion est petite, plus la probabilité qu'il s'agisse d'une tumeur bénigne ou d'un autre type de tumeur maligne est élevée. Néanmoins, la méthode ne peut pas être transférée 1:1 à d'autres organes. Chaque organe a ses propres règles. »
Merci beaucoup pour cette interview.
Profils :
La professeur Dong Yi, MD, PhD, est cheffe du service d'échographie de l'hôpital Xinhua de la faculté de médecine de l'université Jiaotong de Shanghai. Elle est vice-présidente du comité des jeunes de la Chinese Society of Ultrasound in Medicine (CSUM) et de la Shanghai Society of Ultrasound in Medicine. En tant que membre du groupe d'experts des directives et des bonnes pratiques cliniques, elle a co-rédigé les recommandations pour l'échographie de contraste (CEUS) du foie (mises à jour 2020) pour la WFUMB en coopération avec l'EFSUMB, l'AFSUMB, l'AIUM et la FLAUS. Dong Yi a été chercheuse postdoctorale au Massachusetts General Hospital, Harvard Medical School, aux États-Unis, chercheuse à l'université de Pavie en Italie, et au Caritas Hospital, Bad Mergentheim, Allemagne.
Le Dr Christoph Frank Dietrich, MBA, est chef du service médical de la Hirslanden Kliniken Beau Site, Salem et Permanence, Suisse. Il est professeur honoris causa à l'université de Zhengzhou, en Chine. Il s'est spécialisé en médecine interne (1997), en gastroentérologie & hépatologie (2000), notamment avec un Fellowship in Gastroenterology (EBG), en pneumologie (2002), en hématologie et oncologie (2008), en proctologie (2009), en médecine des soins palliatifs (2009) et en médecine gériatrique (2009). Il a été secrétaire honoraire de l'EFSUMB de 2007 à 2011. Il a été président de la Fédération européenne des sociétés d'échographie médicale et biologique (EFSUMB, 2013-2015) et il a été vice-président de la Fédération mondiale d'échographie médicale et biologique (WFUMB) de 2017 à 2019. Sa carrière universitaire est axée sur l'endoscopie et l'échographie. Il a publié plus de 1 100 articles scientifiques et chapitres de livres.