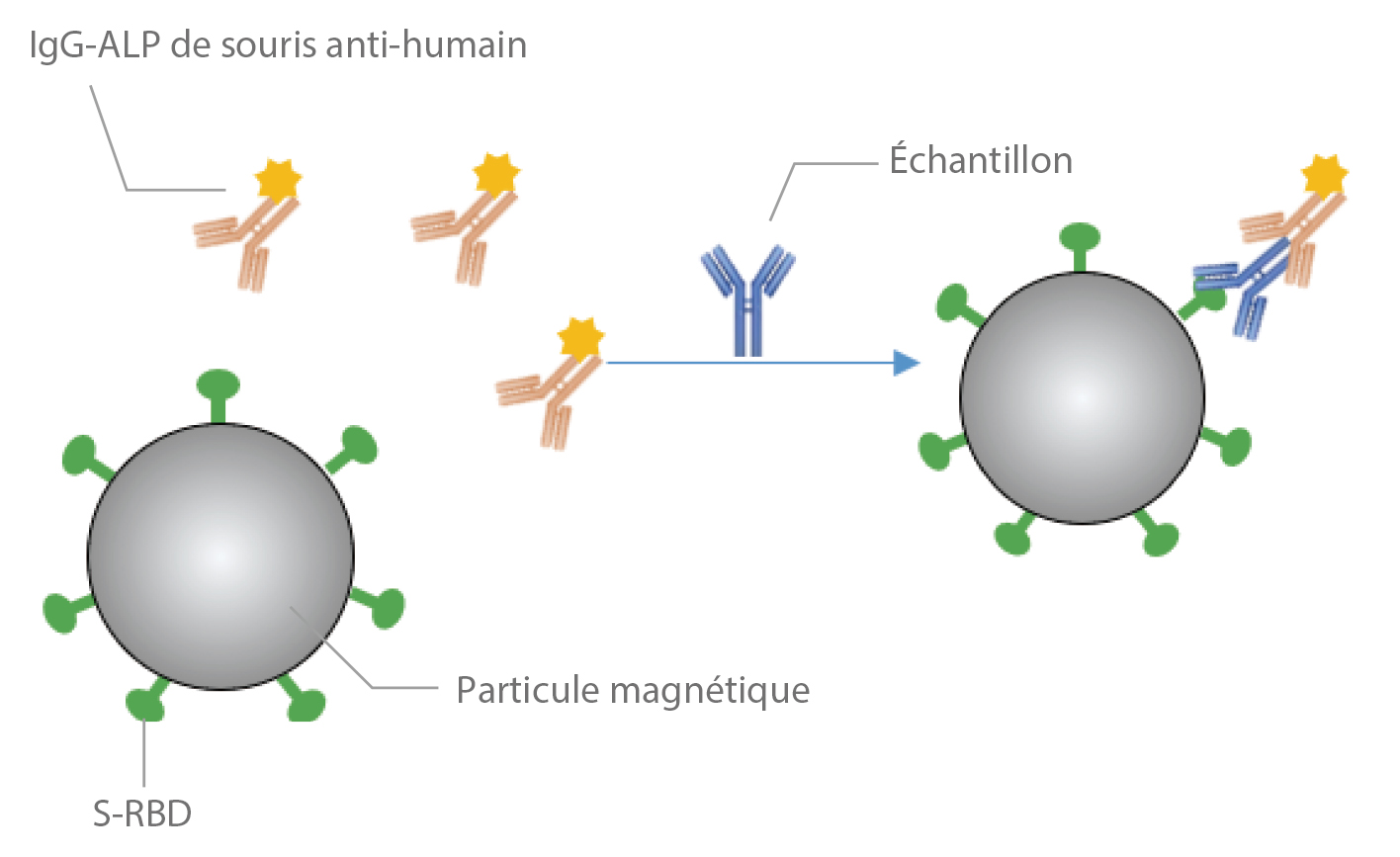
Détection des anticorps neutralisants du SRAS-CoV-2 par immunoanalyse Épisode 1 : S- RBD IgG
Mindray 2021-06-02


Actuellement, il n'existe aucun traitement sûr et efficace des symptômes les plus graves du COVID-19. L'absence de traitement efficace signifie que la vaccination est le seul moyen à notre disposition pour endiguer les impacts dévastateurs de la pandémie. Heureusement, plusieurs types de vaccins différents ont été développés contre le virus SARS-CoV-2.

Le S-RBD du SRAS-CoV-2 se lie à l'ACE2 pour infecter les cellules hôtes. Des études ont montré que les anticorps de neutralisation agissent principalement contre le S-RBD et empêchent le RBD SARS-CoV-2 de se rattacher à l'ACE2. Les vaccins stimulent le système immunitaire pour générer des anticorps neutralisants. Le degré de protection conféré par ces vaccins ou par une infection préalable peut être mis en évidence par la détection d'anticorps neutralisants.
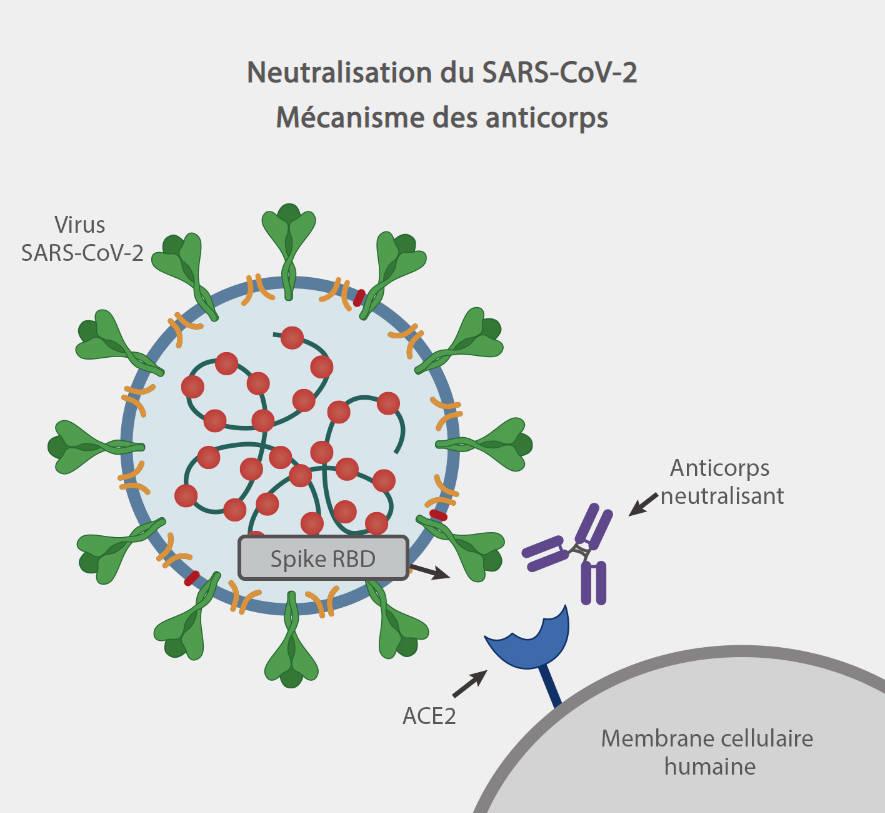
L'identification des anticorps neutralisants peut indiquer
- La réponse immunitaire induite par une infection naturelle et les vaccins (après vaccination).
- La portée pour les récepteurs du vaccin pour connaître la réponse immunitaire réelle avant la vaccination. Il est judicieux pour le gouvernement de distribuer de manière raisonnable les vaccins aux populations les plus exposées, notamment au personnel de santé.
Pourquoi utiliser l'immunoanalyse
L'approche conventionnelle consiste à effectuer un test de neutralisation virale (TNV).
- Méthode standard
- Exigences de biosécurité élevées
- Prend du temps
- Ressources de laboratoire très limitées et très coûteuses
Les inconvénients de la TNV signifient que les dosages immunologiques sont essentiels pour évaluer les vaccins, à la fois dans les essais cliniques et dans le cadre des programmes nationaux de vaccination.
Nous pouvons déduire efficacement le résultat d'un TNV en pratiquant un test de séroneutralisation par réduction des plages de lyse (PRNT).
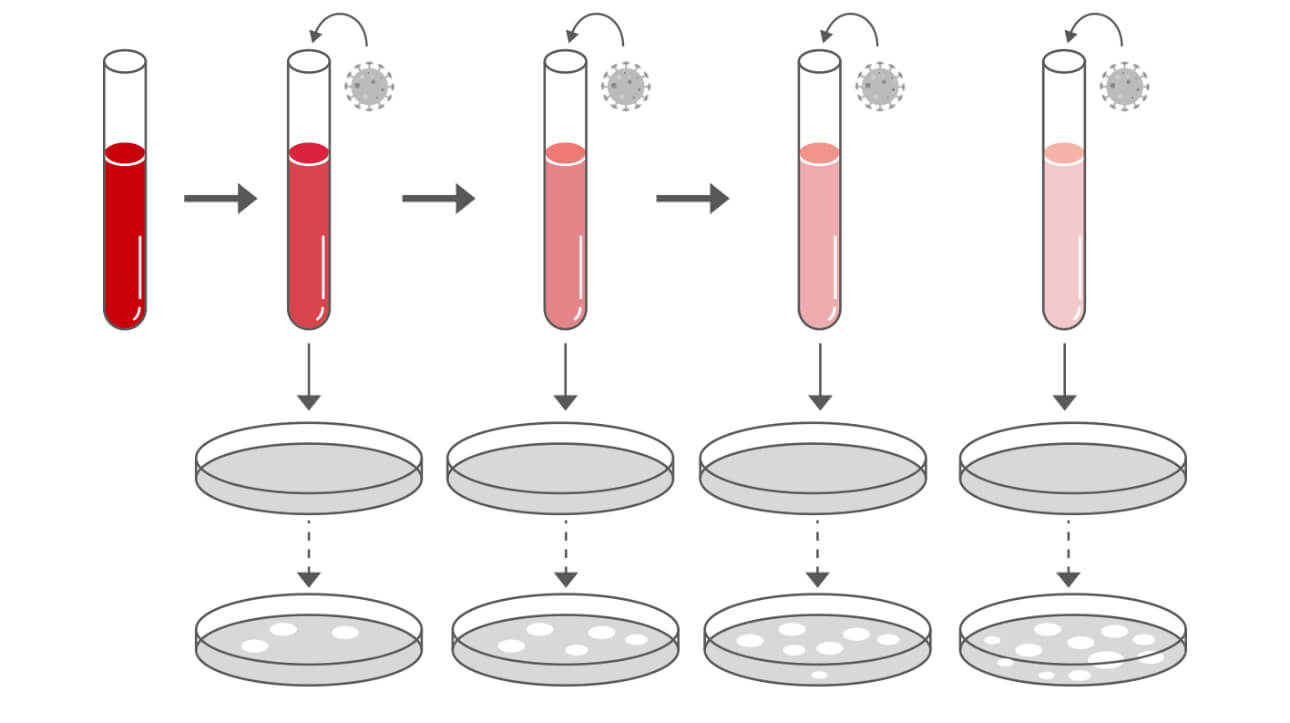
L'immunoanalyse par chimioluminescence est un choix fiable pour contrôler l'efficacité de la vaccination
- L'immunoanalyse peut détecter les anticorps
- Les anticorps de protection ne constituent que 1 à 3 % du total des anticorps en circulation (IgGs)
- Le tableau ci-dessous montre les différences qui existent dans les différentes technologies d'immunoanalyse
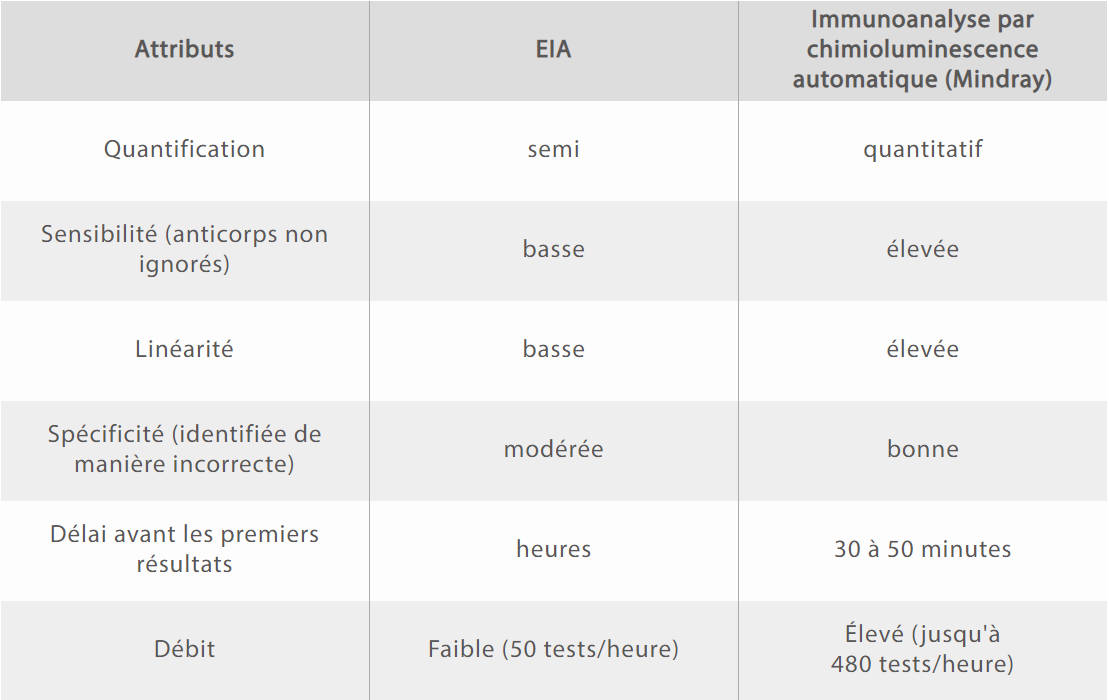
Description des anticorps IgC S-RBD Mindray
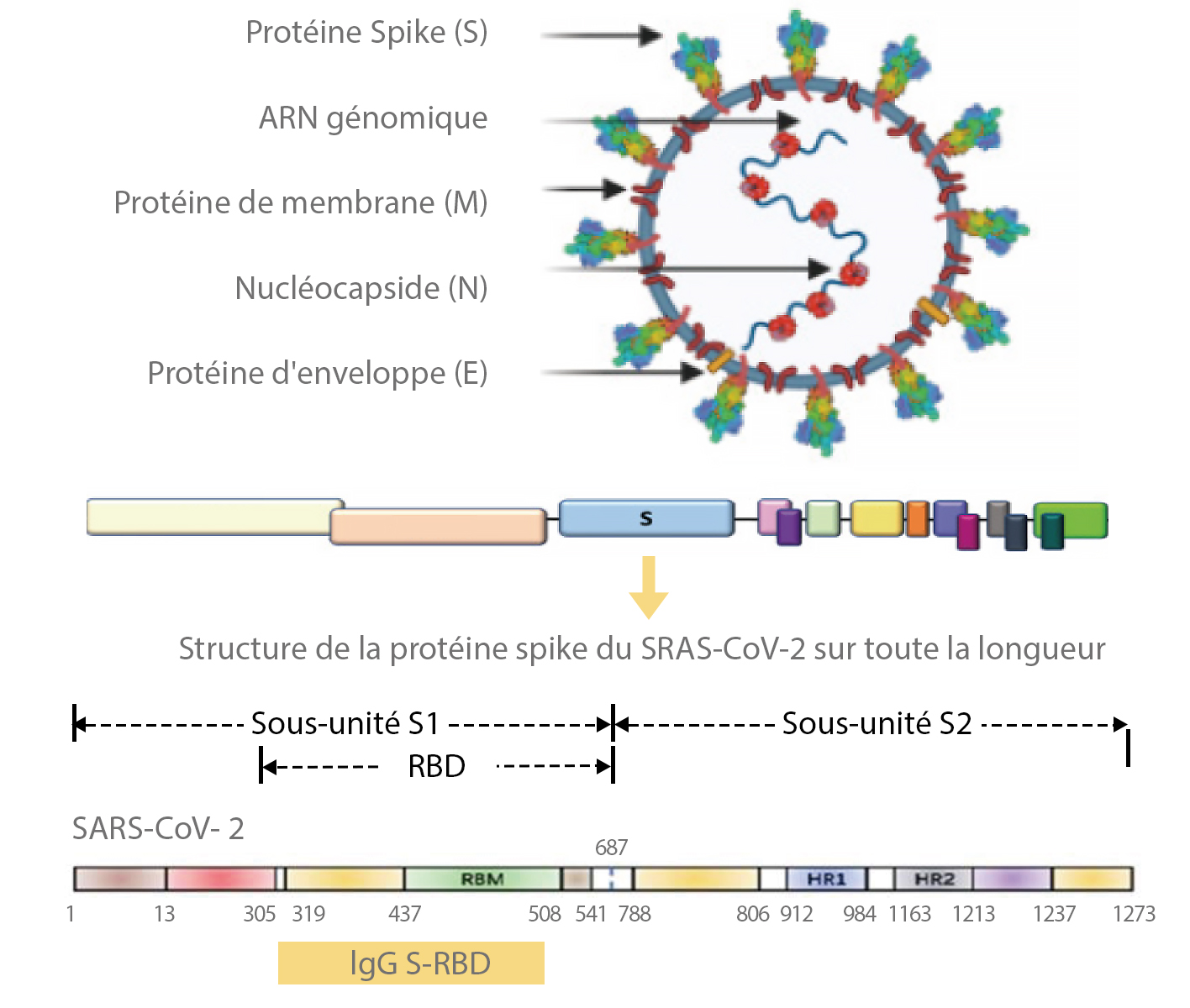
La protéine spike se compose de deux domaines S1 et S2 qui sont responsables de la liaison.
Le domaine S1 contient la protéine du domaine de liaison du récepteur impliquée dans la reconnaissance et la liaison du récepteur de la cellule hôte, tandis que le domaine S2 contient un peptide de fusion putatif ainsi que la répétition heptade HR1 et HR2.
- Le test d'anticorps IgG S-RBD est conçu pour démontrer le mécanisme de protection in vivo
- Il peut détecter de manière spécifique les anticorps neutralisants