Ventilación con protección pulmonar durante la anestesia Folleto de información clínica
Mindray 2020-11-12
La carga de las complicaciones pulmonares posoperatorias (CPP)
Cada año, se realizan en todo el mundo más de 230 millones de procedimientos de cirugía mayor que requieren anestesia general o regional[1].

Durante la etapa intraoperatoria, al iniciar la aplicación de anestesia, el sistema respiratorio del paciente cambiará significativamente. Al principio, los pacientes perderán el conocimiento y el impulso respiratorio central se deprimirá. Entonces, el uso de fármacos bloqueantes neuromusculares paralizará los músculos respiratorios, lo que puede conducir a una disminución significativa de la capacidad residual funcional (CRF) de 15 % a 20 %[3]. La disminución de la CRF frecuentemente causa atelectasia y es uno de los cambios respiratorios más comunes que contribuyen a las CPP durante la anestesia general.
La atelectasia se puede desarrollar en casi el 90 % de los pacientes bajo anestesia general y puede persistir durante el período posoperatorio e incluso hasta siete días después de la cirugía[4].
Para prevenir la atelectasia, a veces se usa un volumen corriente más alto para reexpandir (reclutar) los alvéolos colapsados; sin embargo, esto puede conducir a una sobredistensión o incluso a un volutrauma[5, 6]. Además, el daño por las fuerzas de cizallamiento resultantes de la apertura y el colapso repetitivos de los alvéolos, denominada “atelectrauma”, puede inducir o empeorar las lesiones pulmonares existentes.
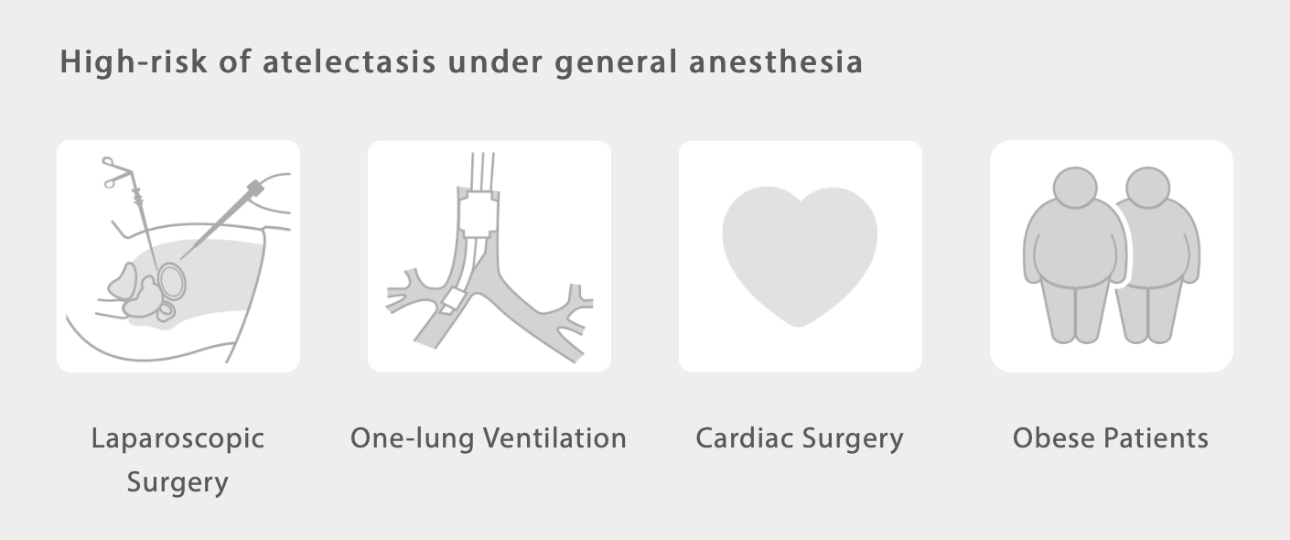
La ventilación de protección pulmonar es ampliamente reconocida como una estrategia eficaz para mantener los alvéolos abiertos y evitar el barotrauma.
Entre las estrategias comúnmente utilizadas se incluyen el volumen corriente bajo, la titulación de PEEP óptima y las maniobras de reexpansión (reclutación) pulmonar[7, 8].
Estrategias de ventilación de protección aplicadas al sistema de anestesia
Volumen corriente bajo
El ensayo clínico MEJORADO sugirió que la ventilación pulmonar protectora y la ventilación no protectora tienen diferentes configuraciones de volumen corriente: 6-8 ml/kg versus 10-12 ml/kg. En retrospectiva, el grupo con el que se usa ventilación de protección pulmonar tiene un menor riesgo de desarrollar CPP, y necesita niveles más bajos de soporte de ventilación y estadías hospitalarias más cortas después de la cirugía[9].
Sin embargo, en un ensayo clínico aleatorizado reciente en adultos que se sometieron a una cirugía mayor, la estrategia de volumen corriente bajo no redujo significativamente los CPP dentro de los primeros 7 días después de la cirugía si la configuración de la PEEP se fijaba en 5 cmH2O, lo que sugiere que es posible que los resultados clínicos no mejoren solo con una estrategia de volumen corriente bajo[10].
PEEP óptima para la atención individualizada del paciente
Un estudio en pacientes con un alto riesgo de atelectasia, como aquellos que se sometieron a una cirugía abdominal laparoscópica, muestra que la configuración individualizada de la PEEP podría reducir la atelectasia posoperatoria y mejorar la oxigenación intraoperatoria con efectos secundarios mínimos[11, 12]. El mismo resultado se puede ver en pacientes obesos, que requieren una PEEP más alta para mantener los pulmones abiertos debido a una presión abdominal más alta[13].
Por lo tanto, se recomienda una titulación óptima de PEEP durante la anestesia para mejorar la función pulmonar durante y después de la cirugía. La PEEP óptima se define como la configuración de la PEEP que conduce a la derivación intrapulmonar más baja sin comprometer el gasto cardíaco[14]. Pero, ¿cómo se realiza la titulación óptima de PEEP para pacientes individuales?
Existen varios métodos de titulación de PEEP comúnmente utilizados por el personal clínico, que incluyen: métodos dirigidos a la distensibilidad pulmonar, mejor oxigenación, técnica guiada de Vds/Vt basada en imágenes y procedimientos dirigidos por presión transpulmonar[11, 12, 15].
Maniobras de reexpansión
La maniobra de reclutamiento es una estrategia dirigida a la reexpansión de los alvéolos colapsados y al aumento de la superficie de intercambio a nivel de la membrana alvéolo-capilar para evitar complicaciones pulmonares intra y postoperatorias[16].
Entonces, ¿cómo se realiza comúnmente la reexpansión pulmonar en el quirófano? En la práctica, se han informado y utilizado una amplia variedad de maniobras de reexpansión, que incluyen la inflación sostenida, el aumento gradual de la ventilación con volumen corriente, el procedimiento de PEEP incremental, etc. La mejor técnica de maniobra de reexpansión puede variar según los pacientes y las circunstancias específicas[7, 17].

En su esfuerzo por usar las mejores prácticas para la seguridad del paciente en entornos de uso de anestesia, Mindray incorpora varias herramientas de ventilación protectoras en los sistemas de anestesia A8/A9, lo que contribuye a una gestión más segura del paciente al reducir el riesgo de CPP y mejorar los resultados del paciente.
Referencias:
[1] Thomas G. Weiser, Scott E. Regenbogen, Katherine D. Thompson, Alex B. Haynes, Stuart R. Lipsitz, William R. Berry, Atul A. Gawande. An estimation of the global volume of surgery: a modelling strategy based on available data. Lancet, 2008, 372: 139-44.
[2] Valentín Mazo, Sergi Sabaté, Jaume Canet, Lluís Gallart, Marcelo Gama de Abreu, Javier Belda, Olivier Langeron, Andreas Hoeft, Paolo Pelosi. Prospective external validation of a predictive score for postoperative pulmonary complications. Anesthesiology, agosto de 2014, 121 (2): 219-31.
[3] Lumb AB, Anaesthesia. En: AB. Lumb Nunn’s Applied Respiratory Physiology, 8.ª edición. Londres: Elsevier, 2016, 291-318.
[4] H. Lundquist, G. Hedenstierna, A. Strandberg, L. Tokics, B. Brismar. CT-assessment of dependent lung densities in man during general anaesthesia. Acta Radiol, 1995, 36: 626-32.
[5] Dreyfuss D., et al. D. Dreyfuss, P. Soler, G. Basset, G. Saumon. High inflation pressure pulmonary edema. Respective effects of high airway pressure, high tidal volume, and positive end-expiratory pressure. Am Rev Respir Dis, 1988, 137: 1159-1164.
[6] Davide Chiumello, Eleonora Carlesso, Paolo Cadringher, Pietro Caironi, Franco Valenza, Federico Polli, Federica Tallarini, Paola Cozzi, Massimo Cressoni, Angelo Colombo, John J. Marini, Luciano Gattinoni. Lung stress and strain during mechanical ventilation for acute respiratory distress syndrome. Am J Respir Crit Care Med, 2008, 178: 346-355.
[7] Andreas Güldner, Thomas Kiss, Ary Serpa Neto, et al. Intraoperative Protective Mechanical Ventilation for Prevention of Postoperative Pulmonary Complications. Anesthesiology, 2015, 123: 692-713.
[8] Emmanuel Marret, Raphael Cinotti, Laurence Berard, et al. Protective ventilation during anaesthesia reduces major postoperative complications after lung cancer surgery. Eur J Anaesthesiol, 2018, 35: 1-9.
[9] Emmanuel Futier, Jean-Michel Constantin, Catherine Paugam-Burtz, et al. A Trial of Intraoperative Low-Tidal-Volume Ventilation in Abdominal Surgery. N Engl J Med, 2013, 369: 428-37.
[10] Dharshi Karalapillai, Laurence Weinberg, Philip Peyton et al. Effect of Intraoperative Low Tidal Volume vs Conventional Tidal Volume on Postoperative Pulmonary Complications in Patients Undergoing Major Surgery: A Randomized Clinical Trial. JAMA, 1 de septiembre de 2020, 324 (9): 848-858.
[11] Zoltán Ruszkai, Erika Kiss, Ildikó László, et al. Effects of intraoperative positive end-expiratory pressure optimization on respiratory mechanics and the inflammatory response: a randomized controlled trial. Journal of Clinical Monitoring and Computing, 2020.
[12] Sérgio M. Pereira, Mauro R. Tucci, Caio C. A. Morais, et al. Individual Positive End-expiratory Pressure Settings Optimize Intraoperative Mechanical Ventilation and Reduce Postoperative Atelectasis. Anesthesiology, 2018, 129: 1070-81.
[13] Francis X. Whalen, Ognjen Gajic, Geoffrey B. Thompson, et al. The Effects of the Alveolar Recruitment Maneuver and Positive End-Expiratory Pressure on Arterial Oxygenation During Laparoscopic Bariatric Surgery. Anesth Analg, 2006, 102: 298-305.
[14] M.J. Civetta, T.A. Barnes, L.O. Smith. “Optimal PEEP” and intermittent mandatory ventilation in the treatment of acute respiratory failure. Respiratory Care, 1975, 20: 551–7.
[15] C. Nestler, P. Simon, D. Petroff, et al. Individualized positive end-expiratory pressure in obese patients during general anaesthesia: a randomized controlled clinical trial using electrical impedance tomography. Br J. Anaesth, 1 de diciembre de 2017, 119 (6): 1194-1205.
[16] L. Magnusson, D. R. Spahn. New concepts of atelectasis during general anaesthesia. British Journal of Anaesthesia, 2003, 91 (1): 61-72.
[17] Paolo Pelosi, Marcelo Gama de Abreu y Patricia RM Rocco. New and conventional strategies for lung recruitment in acute respiratory distress syndrome. Critical Care, 2010, 14: 210.