HemaBook hoofdstuk 7: Hoe D-dimeer in coagulatie correleert met COVID-19?
Mindray 2021-03-03

D-dimeer in COVID-19
Nu COVID-19 de hele wereld nog steeds in zijn greep heeft, blijft een snelle diagnose evenals de prognose en behandeling van COVID-19-patiënten een uiterst belangrijk onderwerp voor clinici. Onlangs hebben wetenschappers ontdekt dat COVID-19 een gastheercelreceptor heeft, Angiotensin Converting Enzyme II[1] of ACE2 genaamd. Met behulp van ACE2 dringt COVID-19 snel het menselijk lichaam binnen door zich in een hoog tempo te reproduceren. Hierbij worden het normale-cellensysteem, het weefselsysteem en het microvasculaire systeem vernietigd, wat uiteindelijk acute longbeschadiging, meervoudig orgaanfalen[2-4] en intravasculaire stolling tot gevolg heeft. Dit was het geval bij 71,4% van de patiënten die stierven aan COVID-19[5]. Het is algemeen bekend dat D-dimeer een belangrijke biomarker is die correleert met hypercoaguleerbaarheid. De relatie tussen D-dimeer en COVID-19 aangetoond is in meerdere klinische studies aangetoond.
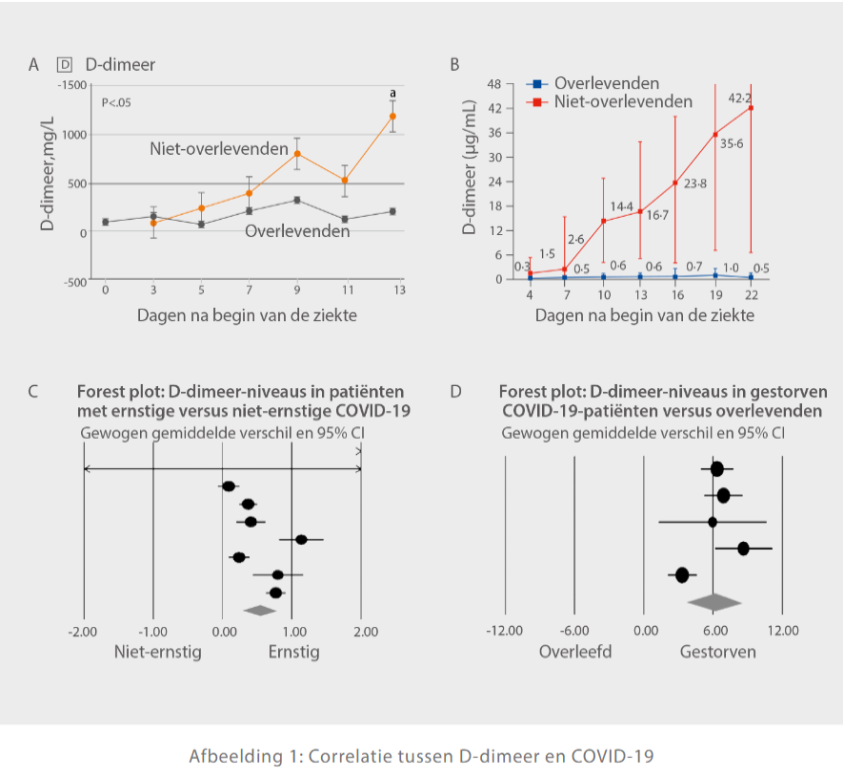
Zoals gepubliceerd op de Jama-website door de groep van Zhi Yong, vond in de groep patiënten die de nieuwe coronavirus-pneumonie niet hebben overleefd, in eerste instantie een verhoging plaats van het D-dimeer-niveau terwijl de ziekte zich ontwikkelde. Op de zevende dag doorbrak het D-dimeer-niveau het normale bereik, tot het zich uiteindelijk stabiliseerde op een hoog niveau [afbeelding 1 A][6]. Ter vergelijking: de groep overlevenden bleef consequent binnen het normale bereik. In een ander artikel in de Lancet wordt ook gesteld dat er een nauwe correlatie bestaat tussen het D-dimeer-niveau en het sterftecijfer van de slachtoffers [afbeelding 1 B][7]. Dezelfde conclusie werd ook getrokken in het onderzoek van Shah, waarin gebruik werd gemaakt van een systematische meta-analysemethode (inclusief resultaten van 18 artikelen en een totaal van 3682 patiënten) om de forest plots te tekenen [afbeelding 1 C, D][8]. Samengevat kan worden gesteld dat of het nu gaat om ernstig zieke of overleden COVID-19-patiënten, het D-dimeer-niveau hoger was dan het niveau dat werd gevonden bij patiënten die niet ernstig ziek waren of de ziekte hadden overleefd.
Toepassing van D-dimeer bij COVID-19-prognose
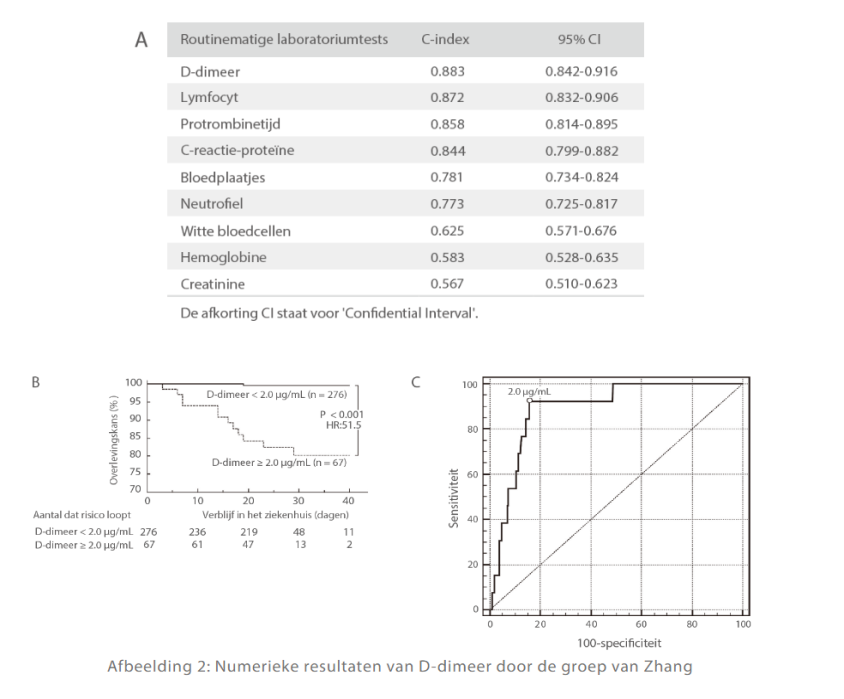
Volgens de studie van Zhang's groep had D-dimeer van alle geteste parameters bij patiënten met COVID-19 de hoogste C-index, wat aangeeft dat deze de hoogste voorspellende toevalligheidsgraad heeft bij routinematige laboratoriumtestmethoden [afbeelding 3 A]. Daarnaast vonden ze ook dat 2 μg/ml van D-dimeer de grenswaarde zou kunnen zijn voor het sterfterisico van COVID-19, aangezien bij DD > 2 μg/ml de overlevingskans drastisch afneemt [afbeelding 2 B]. Bijgevolg baseerden ze zich op de evaluatie van deze waarde en lieten ze zien dat wanneer 2 μg/ml als grenswaarde werd ingesteld, 92,3% van de sensitiviteit en 83,3% van de specificiteit in alle groepen optimaal is [afbeelding 2 C][9].
Er zijn aanwijzingen van een verhoogde incidentie van veneuze trombo-embolie (VTE), waaronder diepe veneuze trombose (DVT) en longembolie (PE), bij patiënten met een ernstige COVID-19-infectie[9] . En D-dimeer kan ook worden gebruikt als een controle-indicator van VTE en PE met een grenswaarde van 0,55 μg/ml. Bovendien vond Yao niet alleen dat patiënten met meer dan 2 μg/ml D-dimeer intensieve zorg en vroege interventie nodig hadden, maar suggereerde hij ook dat een grenswaarde van 1 μg/ml artsen zou kunnen helpen bij het identificeren van patiënten met een slechte prognose[10].
Concluderend kan worden gesteld dat D-dimeer, als een gevoelige controle-index, een enorme klinische waarde heeft bij de behandeling en prognose van COVID-19. In verband met een ongeordende stollingsmicro-omgeving bij patiënten die geïnfecteerd zijn met COVID-19 of die een hoog risico lopen op VTE als gevolg van verminderde activiteit, langere tijd in bed of quarantaine vóór opname in een ziekenhuis, is het regelmatig testen van D-dimeer noodzakelijk voor een snelle monitoring ten behoeve van de behandeling. Hoewel een grenswaarde van 2 ug/ml is bewezen door veel onderzoekers die de behandeling van patiënten monitoren, wordt laboratoria nog steeds geadviseerd om hun eigen standaard te bepalen zodat er rekening kan worden gehouden met variatie in de demografie.
De oplossing van Mindray voor stolling-D-dimeer
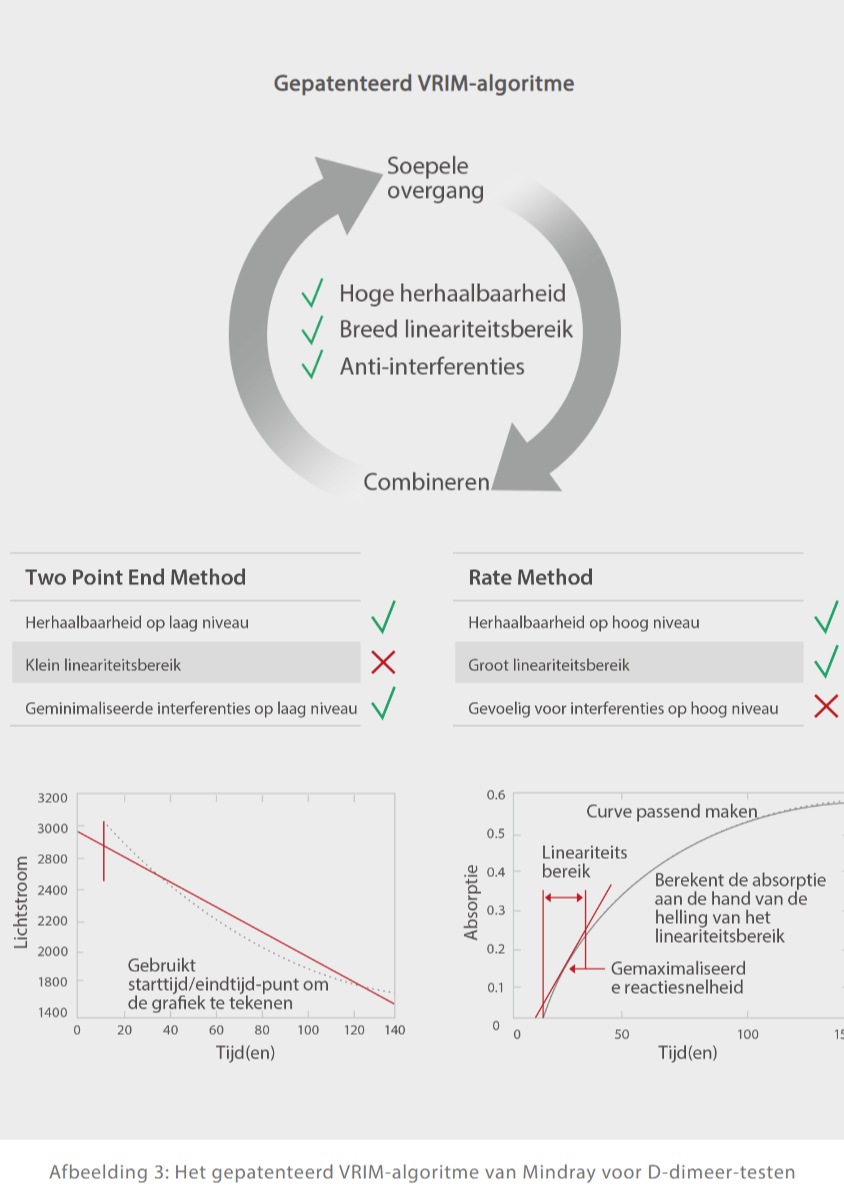
De automatische stollingsanalysatoren C3100 en C3510 zijn uitgerust met zowel klassieke mechanische als optische detectiemechanismen. De mechanische methode is ongevoelig voor interferentie van icterische, lipemische, chylus- en hemolytische samples. Bovendien is het gepatenteerde VRIM-algoritme (VLin-Rate Integrative Method) ontwikkeld om een 'Two Point End Method' bij een lage D-dimeer-concentratie te combineren met een 'Rate Method' bij een hoger niveau [afbeelding 3]. Dit heeft een veel breder lineariteitsbereik van de D-dimeer-resultaten mogelijk gemaakt in vergelijking met andere modellen op de markt [afbeelding 4].
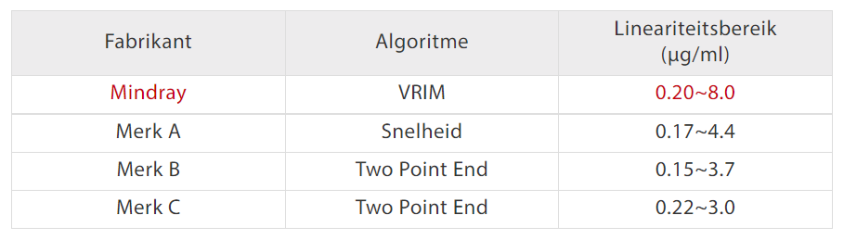
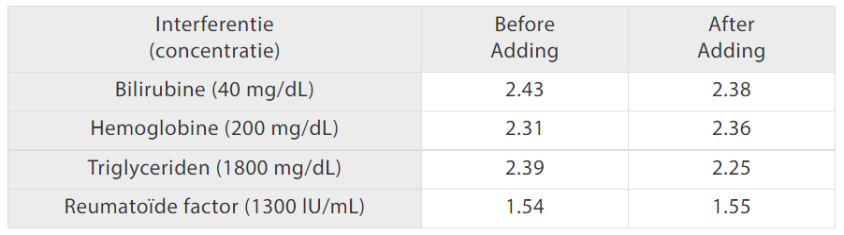
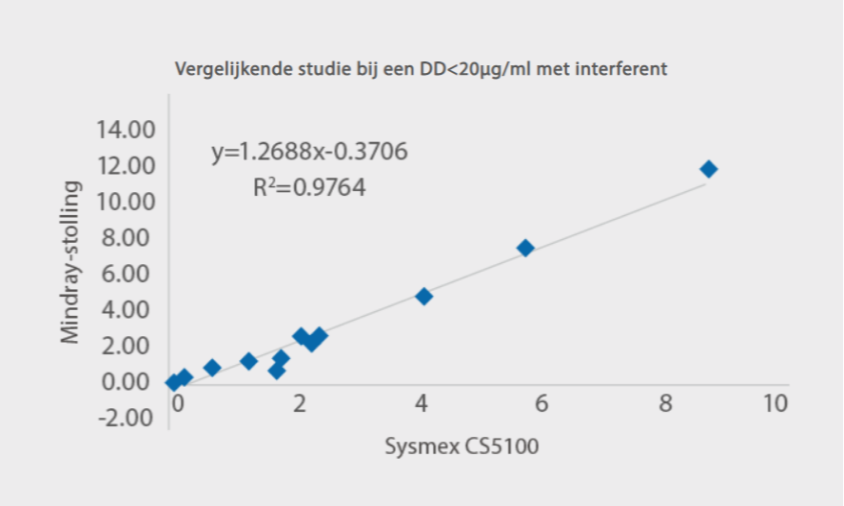
Bovendien is de stollingsoplossing van Mindray voor D-dimeer-testen minder gevoelig voor veelvoorkomende interferenties. Zoals te zien is in afbeelding 5: wanneer aan de serumsamples bilirubine, hemoglobine, triglyceriden en reumatoïde factoren worden toegevoegd in de respectievelijke concentraties, blijven de D-dimeerresultaten op hetzelfde niveau als voorheen. De vergelijkende studie met Sysmex CS5100 heeft ook een goede correlatie aangetoond met R 2> 97% met toegevoegde interferenties.
De D-dimeer-stollingsreagentia van Mindray worden allemaal vervaardigd in gebottelde vloeibare vorm die klaar is voor gebruik (afbeelding 6), terwijl de meerderheid van de stollingstests bestaat uit poeder. Door eenvoudigweg de dop te openen en D-dimeer-reagens op de analysator te laden, kan de voorbereiding snel en eenvoudig worden uitgevoerd op de stollingsanalysatoren van Mindray.
Referenties:
[1] Behl T., Kaur I., Bungau S., Kumar A., Uddin M. S., Kumar C., et al. (2020). The dual impact of ACE2 in COVID-19 and ironical actions in geriatrics and pediatrics with possible therapeutic solutions. Life Sci. 257, 118075. 10.1016/j.lfs.2020.118075.
[2] Tian S, Hu W, Niu L, Liu H, Xu H, Xiao SY. Pulmonary pathology of early phase 2019 novel coronavirus (COVID-19) pneumonia in two patients with lung cancer. J Thorac Oncol. 2020.
[3] Chousterman BG, Swirski FK, Weber GF. Cytokine storm and sepsis disease pathogenesis. Semin Immunopathol. 2017;39(5):517–28.
[4] Ding YQ, Bian XW. Analysis of coronavirus disease-19 (covid-19). Chin J Pathol. 2020;49(00):E003.
[5] Tang N., Li D., Wang X., Sun Z. (2020. b). Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J. Thromb. Haemost. 18, 844–847. 10.1111/jth.14768
[6] Dawei Wang, Bo Hu ,et al. Clinical Characteristics of 138 hospitalized patients with 2019 novel Coronavirus-Infected Pneumonia in Wuhan,China[J]. JAMA. 2020.
[7] Fei Zhou., MD,a., Ting Yu., MD,b. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020 28 March-3 April; 395(10229): 1054–1062.
[8] Shah Siddharth., Shah Kuldeep., Patel Siddharth B., Patel Foram S., Osman Mohammed., Velagapudi Poonam., Turagam Mohit K., Lakkireddy Dhanunjaya., Garg Jalaj.(2020). Elevated D-Dimer Levels Are Associated With Increased Risk of Mortality in Coronavirus Disease 2019: A Systematic Review and Meta-Analysis. Cardiol Rev, 28(6), 295-302. doi:10.1097/CRD.0000000000000330
[9] Zhang Y, Xiao M, Zhang S, et al. Coagulopathy and antiphospholipid antibodies in patients with Covid-19. N Engl J Med. 2020;382:e38.
[10] Simadibrata Daniel Martin., Lubis Anna Mira.(2020). D-dimer levels on admission and all-cause mortality risk in COVID-19 patients: a meta-analysis. Epidemiol Infect, 148(undefined), e202. doi:10.1017/S0950268820002022







